(60)2,4,6-トリニトロフェノールはなぜ強酸なのか
表にこれから説明する化合物の構造とpKaを示しておきます。
フェノールのpKaがほぼ10なのに対し、2,4,6-トリニトロフェノールのそれは0.4、強酸です。構造が大きく違うので化学的性質が異なるのも当然ですが、「共鳴効果が化合物の酸性度に与える影響」について説明するのに絶好の例としてよく知られています。
まず、シンプルにフェノール性水酸基のパラ位にニトロ基が結合している4-ニトロフェノールについて考えましょう。
4-ニトロフェノールでは、図のような共鳴効果で共役塩基が安定化します。これはニトロ基に電子求引性があるためです。電子求引性基は、酸の共役塩基(酸がH+を放出し、分子はマイナスに電荷している状態)の負電荷を分子全体に非局在化させることで、安定化に寄与します。そのため、フェノールに比べ、4-ニトロフェノールのpKaが小さくなり、即ち酸性度が高くなります。
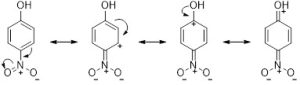
図 4-ニトロフェノールの共鳴構造
共鳴効果はニトロ基がオルト位かパラ位にあるとみられ、これらすべてにニトロ基が結合している2,4,6-トリニトロフェノールのpKaは0.42となります。この化合物は慣用名でピクリン酸として知られ、強酸性化合物というだけでなく引火性・爆発性があり、劇物、危険物第5類に指定されています(融点:122 ℃,沸点:325 ℃,発火点:322 ℃)
ちなみに、1-ナフトールはフェノールより若干酸性度が高くなりますが、これは共鳴構造がベンゼンよりもナフタレンのほうが若干安定であるためと考えられます。
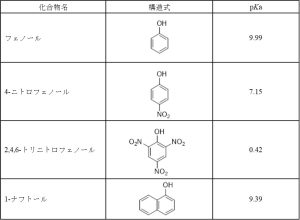
表 フェノール類のpKa1)と構造式
【引用文献】
1) Haynes W. M. eds. CRC Handbook of Chemistry and Physics, 97th Edition 2016-2017, pp.5-88 – 97, CRC Press (2016).


